北理工團(tuán)隊(duì)在抗SARS-CoV-2新型PROTAC分子設(shè)計(jì)及機(jī)制研究中取得重要突破
供稿、供圖:化學(xué)與化工學(xué)院 編輯:田柳
近日,北京理工大學(xué)化學(xué)與化工學(xué)院梁建華教授、孟子暉教授、于明加副研究員所帶領(lǐng)的團(tuán)隊(duì)在抗SARS-CoV-2藥物研發(fā)領(lǐng)域取得重要進(jìn)展,相關(guān)成果以“Structure-Informed Design of High-Cooperativity PROTAC Targeting SARS-CoV-2 RdRp via Click Chemistry and Enhanced Sampling Simulations”為題發(fā)表于國(guó)際權(quán)威期刊《Journal of Medicinal Chemistry》(《藥物化學(xué)雜志》)。該研究創(chuàng)新性地開發(fā)出高協(xié)同性PROTAC分子,為抗新冠病毒及變異株藥物研發(fā)提供了全新策略和候選分子。
新冠病毒(SARS-CoV-2)及其變異株的持續(xù)傳播給全球公共衛(wèi)生帶來嚴(yán)峻挑戰(zhàn),傳統(tǒng)抗病毒藥物常面臨耐藥性突變、作用持續(xù)時(shí)間短等問題。RNA依賴的RNA聚合酶(RdRp)作為新冠病毒復(fù)制過程中的關(guān)鍵酶,具有高度保守性且無人類同源物,是抗病毒藥物研發(fā)的理想靶點(diǎn)。然而,現(xiàn)有RdRp抑制劑多為底物競(jìng)爭(zhēng)性抑制劑,存在劑量依賴型療效和耐藥風(fēng)險(xiǎn)等局限。
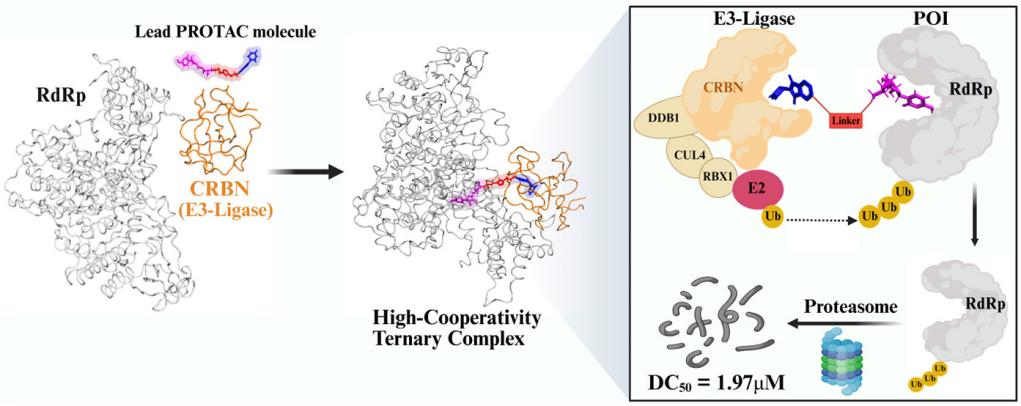
圖 1. 本研究總體設(shè)計(jì)思路
針對(duì)這一難題,團(tuán)隊(duì)提出結(jié)構(gòu)引導(dǎo)的PROTAC設(shè)計(jì)策略,將臨床驗(yàn)證的RdRp抑制劑(莫諾拉韋、瑞德西韋等)與E3泛素連接酶配體通過點(diǎn)擊化學(xué)技術(shù)進(jìn)行精準(zhǔn)偶聯(lián)。團(tuán)隊(duì)通過整合分子模擬、合成化學(xué)與生物驗(yàn)證等多學(xué)科手段,從600個(gè)候選分子中篩選出最優(yōu)化合物PROTAC 10。該分子以莫諾拉韋為靶向彈頭、CRBN為E3連接酶配體,通過三唑-烷基雜化連接子構(gòu)建,展現(xiàn)出優(yōu)異的靶向降解性能。
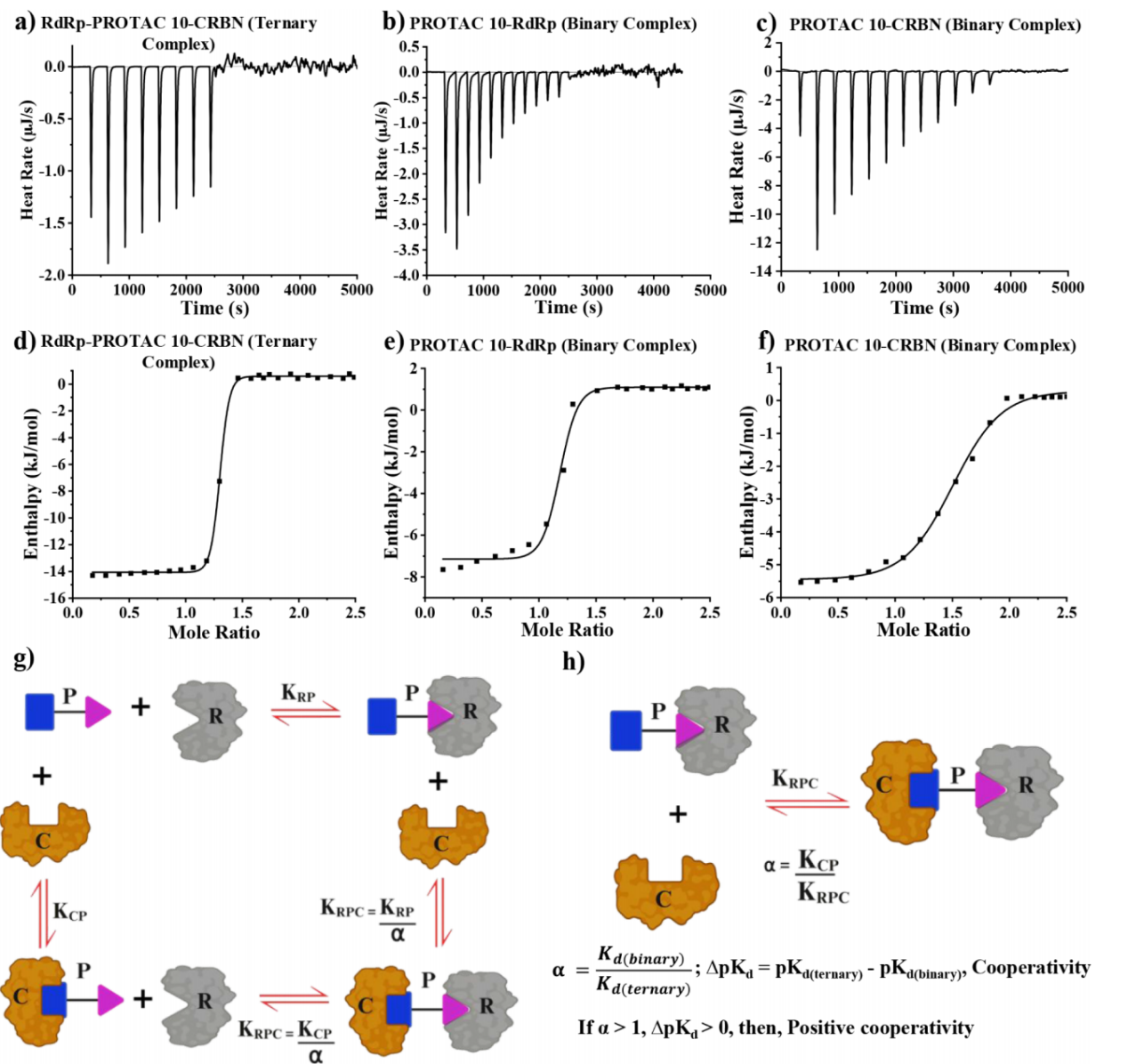
圖 2. 先導(dǎo)化合物PROTAC 10誘導(dǎo)E3連接酶與靶蛋白(POI)形成三元復(fù)合物的結(jié)合及熱力學(xué)分析
機(jī)制研究表明,PROTAC 10具有顯著的正協(xié)同效應(yīng)(α=45.9),能高效誘導(dǎo)RdRp與CRBN形成穩(wěn)定三元復(fù)合物(結(jié)合自由能ΔGTER=-247 kcal/mol),通過泛素-蛋白酶體途徑特異性降解RdRp。細(xì)胞實(shí)驗(yàn)驗(yàn)證,其半數(shù)降解濃度(DC50=1.97 μM)低于半數(shù)抑制濃度(IC50=3.12 μM),實(shí)現(xiàn)降解驅(qū)動(dòng)的抗病毒活性,且對(duì)CRBN經(jīng)典底物無明顯影響,展現(xiàn)出良好的靶向選擇性。此外,該分子通過獨(dú)特的“變色龍”行為,在非極性環(huán)境中形成分子內(nèi)氫鍵降低極性表面積,有效提升細(xì)胞滲透性,解決了傳統(tǒng)PROTAC分子量大、膜通透性差的關(guān)鍵難題。
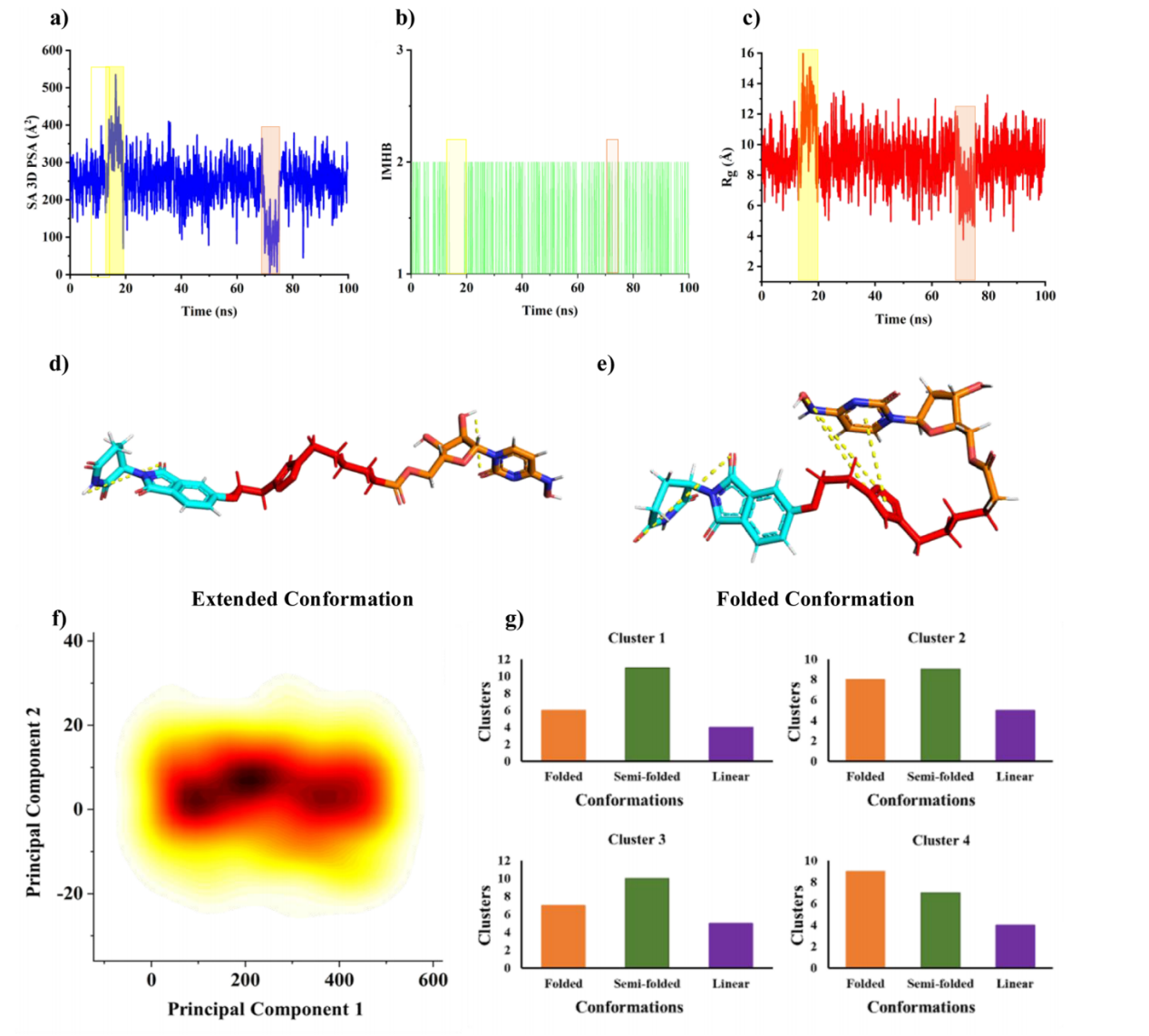
圖 3. PROTAC 10的折疊構(gòu)象與伸展構(gòu)象具有分子特性的變色龍行為
為深入解析作用機(jī)制,團(tuán)隊(duì)開展全原子動(dòng)力學(xué)模擬,捕捉到PROTAC 10化合物誘導(dǎo)與RdRp、CRBN形成三元復(fù)合物的動(dòng)態(tài)形成過程。該模擬明確了PROTAC技術(shù)通過“雙配體識(shí)別-連接子構(gòu)象調(diào)整-蛋白界面錨定”三步,驅(qū)動(dòng)RdRp與CRBN形成穩(wěn)定復(fù)合物,為其降解活性提供了原子水平的機(jī)制證據(jù)。
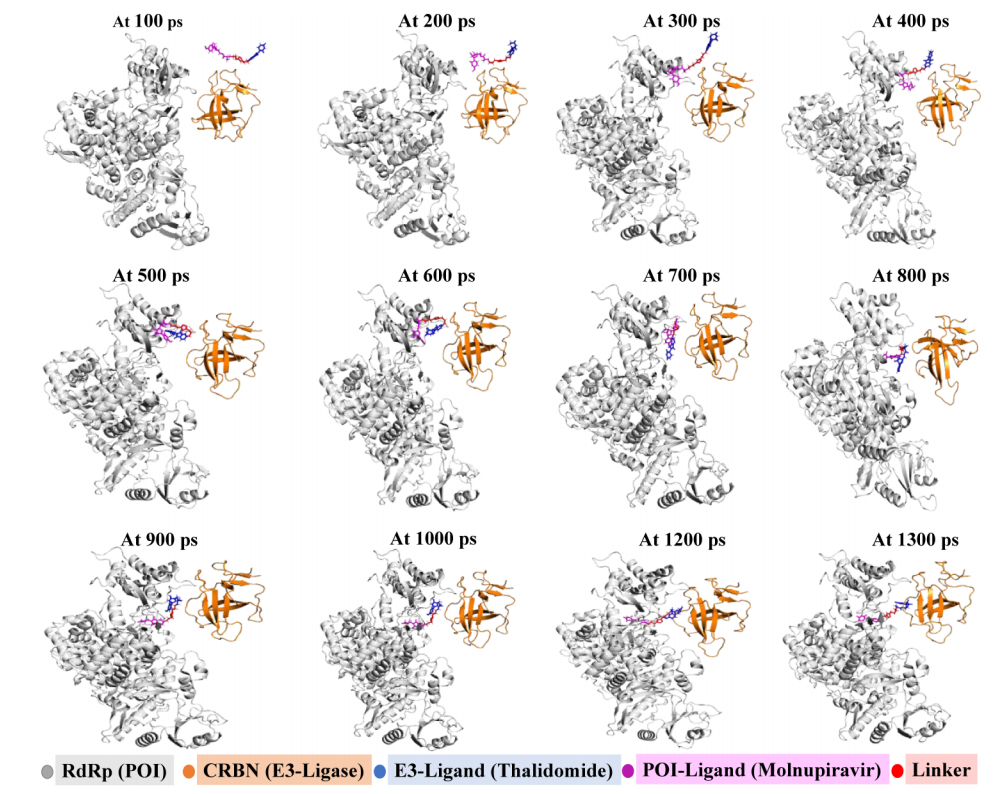
圖 4. PROTAC 10 誘導(dǎo)RdRp(灰色)與CRBN(橙色)形成三元復(fù)合物的1300 ps動(dòng)態(tài)模擬軌跡圖
該研究首次報(bào)道了靶向SARS-CoV-2 RdRp的PROTAC分子,其創(chuàng)新設(shè)計(jì)策略不僅突破了傳統(tǒng)抑制劑的作用局限,為抗新冠病毒藥物研發(fā)開辟了新路徑,也為泛冠狀病毒降解劑的開發(fā)提供了重要參考。所開發(fā)的PROTAC 10具有合成簡(jiǎn)便、靶向性強(qiáng)、抗病毒譜廣等優(yōu)勢(shì),有望成為對(duì)抗新冠病毒變異株的潛在候選藥物。
論文第一作者為北京理工大學(xué)化學(xué)與化工學(xué)院博士生Kiran Shehzadi,梁建華教授、孟子暉教授、于明加特別副研究員和Irfan Muhammad教授為共同通訊作者。該研究得到國(guó)家自然科學(xué)基金、北京理工大學(xué)學(xué)者研究基金等項(xiàng)目支持,北京理工大學(xué)為第一通訊單位。
論文信息:Kiran Shehzadi#, Yue Ran, Iqra Kalsoom, Jingyue Dong, Peifeng Gao, Irfan Muhammad*, Ming-Jia Yu*, Zihui Meng*, Jian-Hua Liang*. Structure-Informed Design of High-Cooperativity PROTAC Targeting SARS-CoV?2 RdRp via Click Chemistry and Enhanced Sampling Simulations. Journal of Medicinal Chemistry, 2025, DOI: 10.1021/acs.jmedchem.5c02065.
附通訊作者簡(jiǎn)介:
通訊作者:
梁建華,北京理工大學(xué)教授,醫(yī)藥分子科學(xué)與制劑工程工信部重點(diǎn)實(shí)驗(yàn)室副主任,新藥創(chuàng)制與綠色合成研究所所長(zhǎng),研究方向?yàn)橹卮蠹膊∠嚓P(guān)的新藥創(chuàng)制;
孟子暉,北京理工大學(xué)教授,博士生導(dǎo)師,應(yīng)用化學(xué)研究所所長(zhǎng),研究方向?yàn)獒t(yī)用劑型材料的研發(fā);
于明加,北京理工大學(xué)副研究員,新藥創(chuàng)制與綠色合成研究所副所長(zhǎng),研究方向?yàn)榭共《尽⒖寡椎戎卮蠹膊∠葘?dǎo)化合物的智能設(shè)計(jì)與開發(fā)。
本研究受到國(guó)家自然科學(xué)基金(U1530141)和國(guó)家自然科學(xué)基金青年科學(xué)基金(32201053)、北京理工大學(xué)青年教師學(xué)術(shù)啟動(dòng)計(jì)劃(3100012222222)資助。
(審核:王振華)





